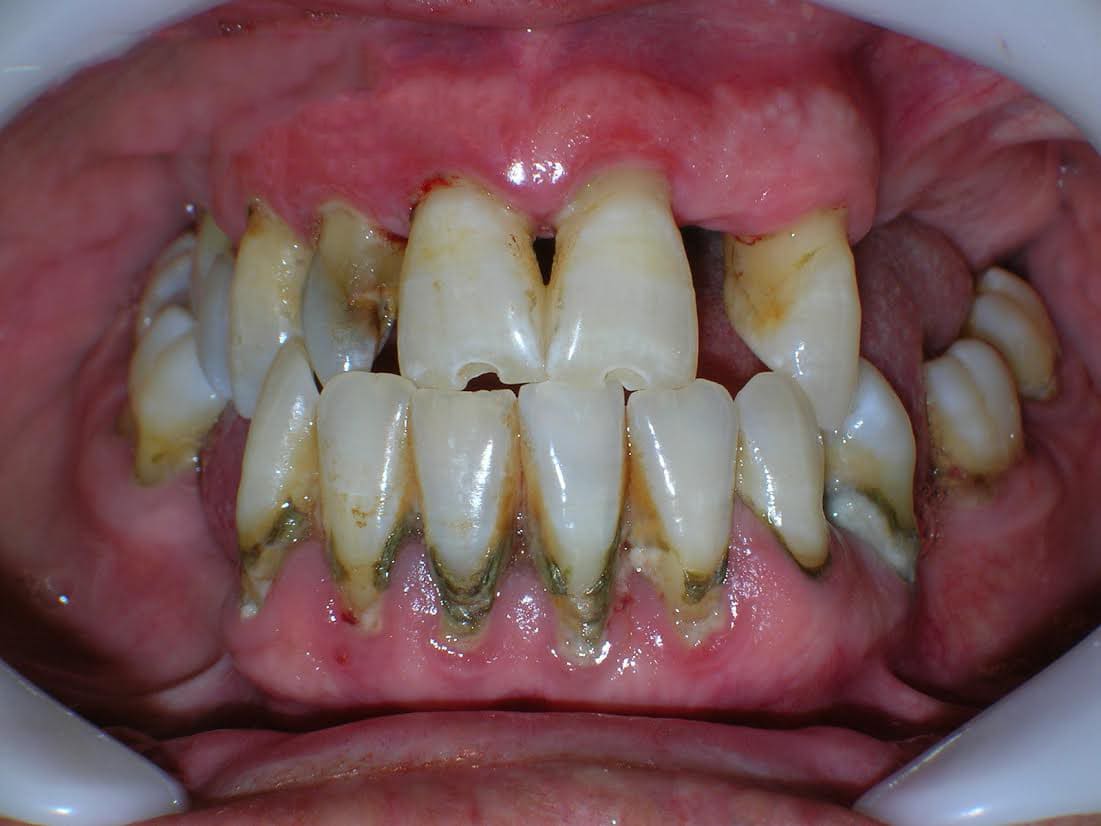
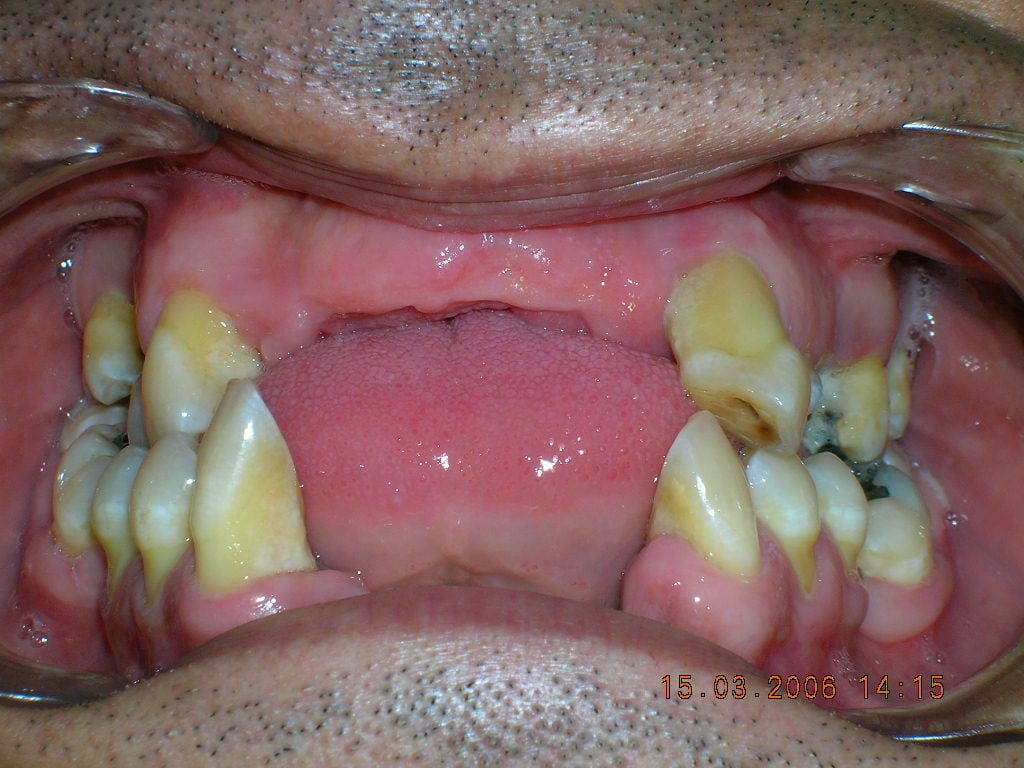
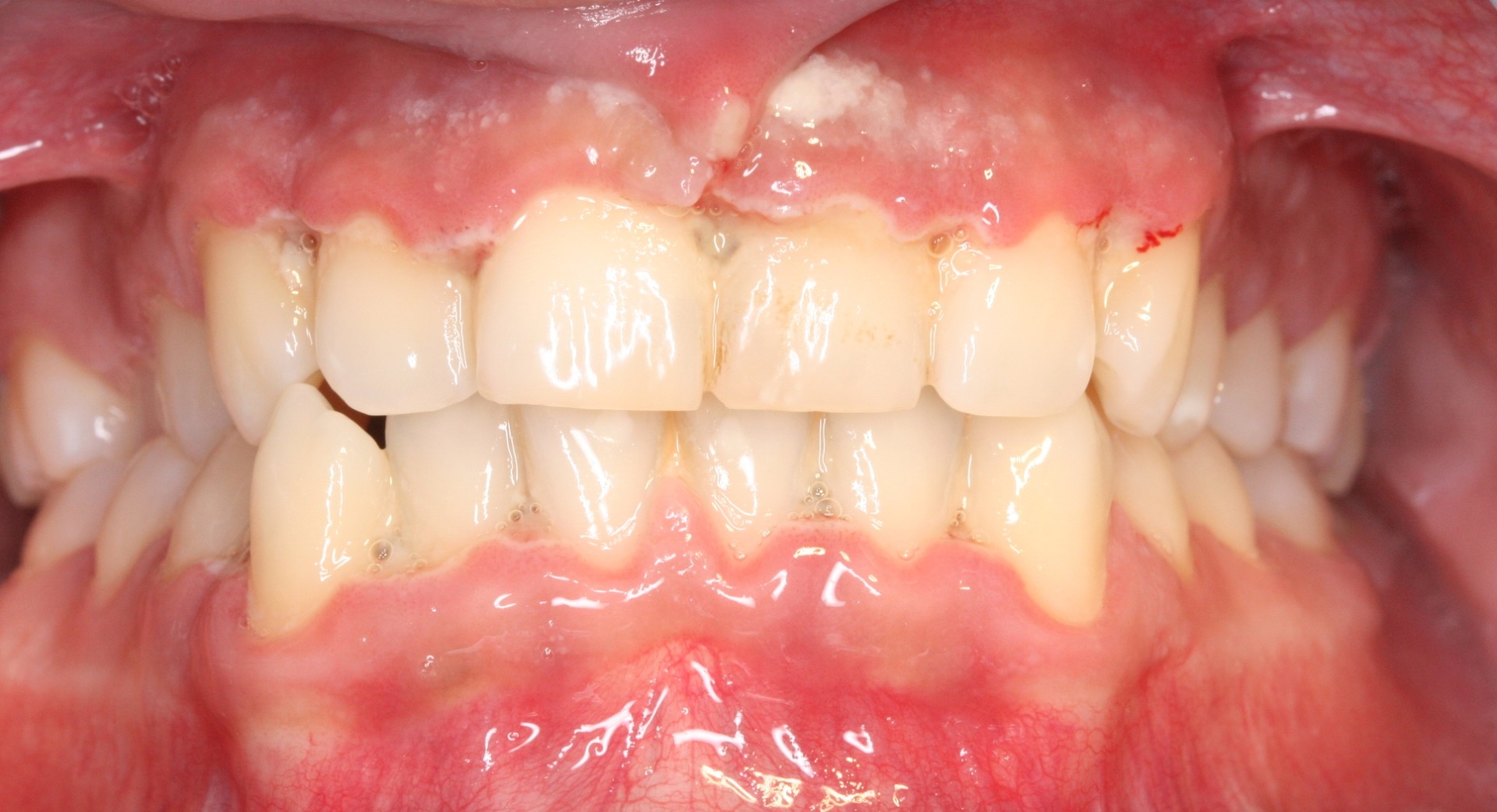
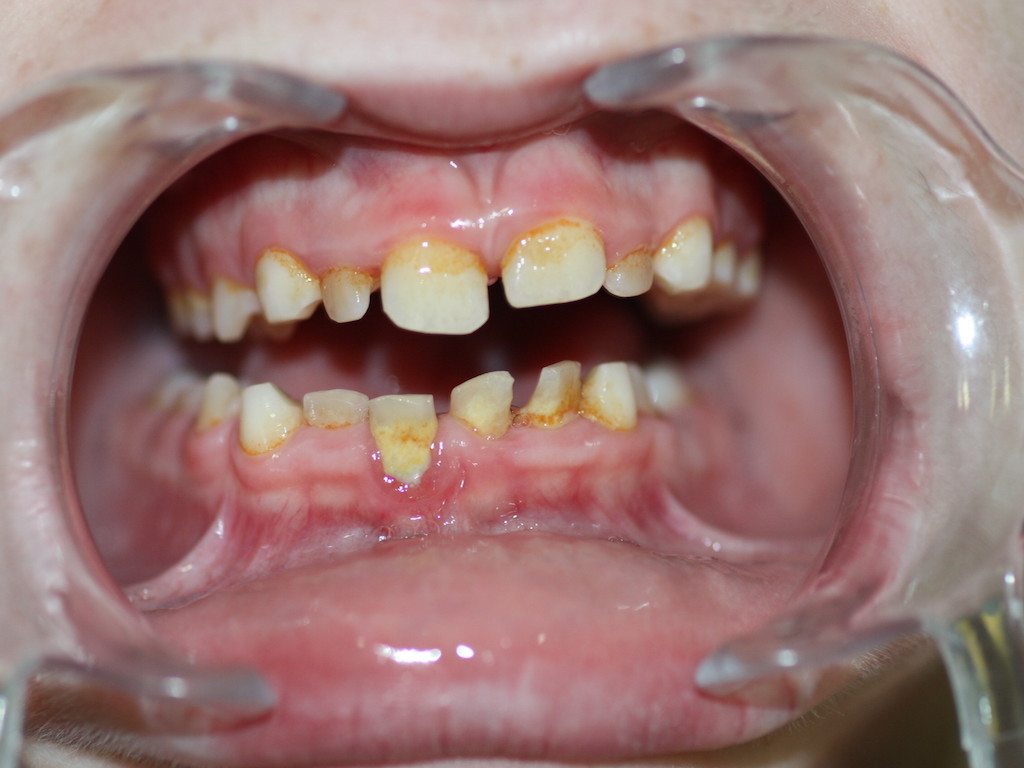
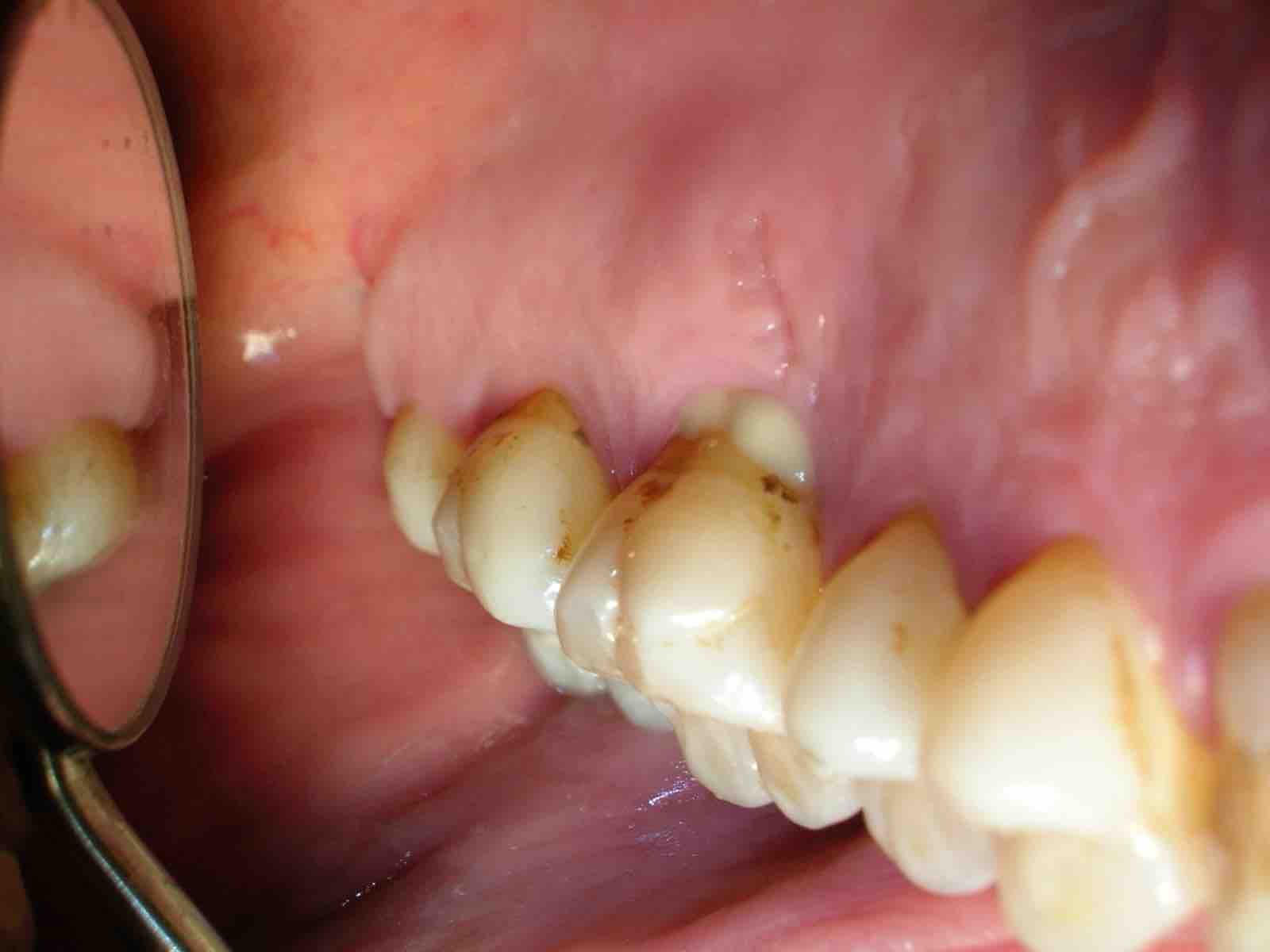
Es una enfermedad infectocontagiosa, causada por bacterias que, en sujetos susceptibles, produce inflamación de los tejidos que sujetan el diente o la muela al hueso y al ligamento periodontal. Generalmente el enfermo antes tuvo una gingivitis. Profundización del Surco Gingivodentario: el surco es el espacio que hay entre el diente y la encía, parecido a lo que sucede con la piel y la uña. Cuando una persona presenta una encía sana, éste mide entre uno y dos milímetros de profundidad. Para saber esto, el paciente debe ir al dentista y someterse a un examen, en el que se le introduce una sonda periodontal en dicha cavidad. Si ésta mide más de tres milímetros, hay una profundización patológica, que casi siempre corresponde a un Saco Periodontal. La presencia de agentes patógenos y una mala higiene son las causantes de la alteración del surco. Con esta profundización hay mayores posibilidades de que se aloje placa bacteriana y sarro. El saco periodontal es una señal típica de la Periodontitis. Este síntoma es muy difícil de advertir. Sólo un odontólogo puede determinar si está presente. Por ello, se recomienda que el paciente le solicite a su dentista un sondaje periodontal. Enrojecimiento de las encías, sangramiento, edema (aumento de volumen), acumulación de placa y sarro. En principio, la inflamación crónica constituye un modo de defensa del individuo, en un esfuerzo por deshacerse de las bacterias. El problema es que la inflamación sostenida paulatinamente va contribuyendo a degradar los tejidos del propio organismo, principalmente la encía y el hueso. Este último tejido es el que más sufre, ya que no responde bien frente a los estímulos inflamatorios crónicos; tiende a reabsorberse. Por lo tanto, conforme pasa el tiempo y se mantiene la inflamación crónica de la periodontitis, el hueso se va destruyendo. Esto es grave, ya que el hueso es el que en esencia, sujeta los dientes en su lugar, mediante un tejido blando que actúa como unión a la raíz: El ligamento periodontal. Si desaparece el hueso, el ligamento periodontal también lo hará, y el diente se irá quedando sin sustento. Como un edificio al que se le horadara la tierra alrededor de sus bases, el diente va perdiendo soporte. Según la velocidad de destrucción del hueso (lo que varía de un sujeto a otro, aunque por lo general es lento), pueden comenzar a verse algunos signos: La recesión de la encía que deja al descubierto las raíces (la encía se va recogiendo a consecuencia de la desaparición del hueso) y más adelante, la movilidad del diente. Antes de esto signos, la encía ha mostrado otros; como enrojecimiento, hinchazón y sangramiento. En ocasiones puede haber supuración (fig 10). Normalmente no hay dolor, por lo que el paciente suele no darse cuenta de que está sufriendo la destrucción de sus tejidos. Incluso, el signo más decisivo, la presencia de la “bolsa” o “saco” periodontal, sólo es demostrable mediante un sondaje periodontal, que es realizado por un Odontólogo. Este consiste en la profundización patológica del surco gingivodentario. El surco gingivodentario es lo que se forma en la zona en que la encía se une al diente, es un pliegue de mucosa que forma el surco, dejando por fuera la encía y por dentro el diente. Normalmente es poco profundo; 1 o 2 milímetros a lo sumo. Para que se entienda mejor, se parece un poco a la manera como la piel bajo la uña se adhiere a ésta, dejando un pequeño surco que está presente incluso en aquellos que usan las uñas cortas. Pues bien, en la Periodontitis, el surco gingivodentario se va profundizando producto de la inflamación y la acumulación de bacterias y toxinas, haciendo que la unión de la encía al diente se vaya “escapando” más abajo, en dirección a la raíz, y con ello, este surco se hace más profundo, llamándosele entonces bolsa o saco periodontal. Si la enfermedad continúa, a la larga, la pérdida de los tejidos que sujetan el diente será tan grave, que se comenzarán a perder los dientes. El paciente puede llegar a perder la totalidad de sus piezas dentarias. Además de la pérdida de dientes, el paciente puede sufrir graves alteraciones estéticas, y es común que sufra de halitosis (mal aliento). (fig 11). Según el grado de destrucción del hueso que sujeta los dientes, la periodontitis puede clasificarse en Incipiente, moderada o severa. A la vez, dependiendo si están afectados muchos o pocos dientes, puede ser generalizada o localizada. Factores de riesgo de la Periodontitis.
Existen factores que hacen a una persona más susceptible de enfermar de Periodontitis. El factor más conocido es la mala calidad de la higiene. Como el factor inicial de la enfermedad son ciertas bacterias, mientras más cantidad de ellas exista, mayor es la posibilidad de enfermar. Si el paciente tiene mala higiene, no se cepilla correctamente y no usa seda dental, la población de bacterias aumentará. El tabaquismo es otro factor muy importante: El cigarrillo modifica la irrigación sanguínea, disminuyendo la cantidad de sangre que llega a la encía, perjudicando así a los tejidos y permitiendo el desarrollo de las bacterias patógenas. Lo insólito es que por el mismo efecto isquémico del tabaco (el disminuir el aporte de sangre), hace que los signos de la inflamación disminuyan, por lo tanto, las encías no se ven tan enrojecidas, hinchadas ni sangrantes, lo que puede transmitir una falsa sensación de salud. Sólo un sondaje periodontal hará evidente el daño La herencia influye. La periodontitis en sí no es hereditaria, pero el riesgo de enfermar relacionado a las características de la inflamación que opone el paciente, puede tener un patrón hereditario.
Periodontitis asociada a Enfermedades generales o sistémicas.
Ciertas enfermedades generales favorecen la aparición de Periodontitis, siendo la más común, la diabetes. También hay trastornos como las leucemias, el Síndrome de Down, Síndrome de Papillon-Lefèvre, Síndrome de Cohen y la Hipofosfatasia; que cursan frecuentemente con Periodontitis.